クロマトグラフィーによるウイルスクリアランス:
至適条件と担体の寿命を予測
日米EU医薬品規制調和国際会議(ICH)のウイルスクリアランスのガイドラインQ5Aには、クロマトグラフィーカラムを繰返し使用すると、ウイルス除去能力が徐々に低下するおそれがあると記載されています。この問題を解消するため、生物およびバイオテクノロジー製剤のメーカーは、未使用のクロマトグラフィー担体と経年したクロマトグラフィー担体を用いて、ウイルスクリアランス試験を実施しました。ここ数年は、クロマトグラフィーカラムのウイルスクリアランスを予測する試みが行われています。迅速に測定できるカラムの性能指標とカラムのウイルス除去能力との間に相関関係があれば非常に有利で、PAT(Process Analysis Technology)の方針とも一致します。
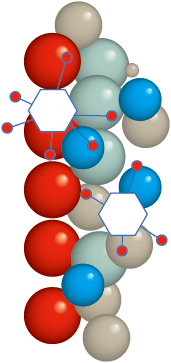
図1. ウイルスとタンパク質が結合したHIC担体との結合模式
ウイルスクリアランスに影響を及ぼす因子
ウイルスと担体表面との相互作用についてはあまりよく理解されていません。タンパク質の濃度、プロダクトの特性(疎水性など)、不純物の性質や量などの因子がウイルスクリアランスに影響を及ぼすと考えられます。疎水相互作用クロマトグラフィー(HIC)の場合、カラム上にタンパク質が蓄積すると、ウイルスと官能基との相互作用が促進されます(図1参照)。HICカラム寿命の指標を調べた結果、90サイクル使用してもプロダクトの収率、凝集、Protein A漏れ成分の除去能は変わらないことが分かりました。エンベロープウイルスの除去能も変わりませんでしたが、非エンベロープウイルスSV40の除去能は経時的に低下しました1。
陰イオン交換クロマトグラフィーによるウイルス除去は、疎水相互作用クロマトグラフィーによる除去に比べて操作が多少簡単です。未使用のクロマトグラフィー担体も経年したクロマトグラフィー担体も、プロダクトをカラムに通過させた後、エンベロープウイルスを完全に除去できました。しかし、非エンベロープウイルスではそうはいきませんでした。非エンベロープウイルスは未使用の担体では良好に除去できましたが、経年した担体では十分に除去できませんでした。このような差が生じる理由は明らかでなく、最近発表された以下の研究結果とも食い違っています。
Protein A Sepharose™に関する研究とQ Sepharose™ Fast Flowに関する研究で、ある特定の条件下で、ウイルスクリアランス能力の低下を製造中に迅速に測定できる指標が見つかりました。前者はFDAのモノクローナル抗体部門が実施した研究で2、Q-PCR(定量PCR)を用いてProtein A Sepharose™でのレトロウイルスの減少を評価しました。 ウイルスクリアランス能力の低下の優れた指標は、抗体の精製量とカラムの通過成分量でした。一方、溶出液中の不純物含有量は良い指標とはなりませんでした。レトロウイルスクリアランス能力の低下が見られるかなり前から、収率が低下していました。
Protein A Sepharose™カラムにおけるウイルスクリアランス能力の低下については収率が優れた指標となりますが、陰イオン交換カラムをフロースルーモードで使用した場合は、収率に関する経時変化だけでは、十分な指標とはなりませんでした。バンド拡散(理論段数相当高さ (HETP)で評価)、DNAクリアランス、背圧上昇はいずれもカラム性能を示す指標でした。フロースルーモードの陰イオン交換カラムを、推奨の洗浄バッファーで洗浄し、HETP、DNAクリアランス、背圧を定期的にモニターしている場合、バリデートされた担体の設定期限まではウイルスクリアランスの評価をする必要はないという結論に達しました3。
この広範囲な研究については、FDAのモノクローナル抗体部門、Genentech社、Cytiva社の共著で論文を発表しています。エンベロープウイルス(X-MuLV)と2種類の非エンベロープウイルス(SV40、MMV)のクリアランスをPCRで評価しました。クロマトグラフィーカラムを繰返し使用する場合に、ウイルスクリアランス能力に明らかに影響を及ぼす因子は洗浄です。Norlingらの論文によると、洗浄しなかった場合と、担体を劣化させるバッファーで洗浄した場合には、ウイルスクリアランス能力が低下します。
フロースルーモードでの陰イオン交換クロマトグラフィーに関する別の研究では、ウイルスクリアランスが一般的なマトリックスでのアプローチによって検討されました。この研究は、Sherrie Curtisがプロセスバリデーションに関する学会で最近発表したものです4。SV40とX-MuLVは、pH 7.0~8.0、導電性4.6~12 mS/cm、担体の結合容量 < 200 g/l、線流速500 cm/h以内、ベッド高11 cmという条件で確実に除去されることが示されました(> 4 log10)。
まとめ
イオン交換やProtein Aクロマトグラフィーは、バイオ医薬品の精製に広く用いられています。迅速に測定できるインプロセスパラメータとウイルスクリアランスに相関性があれば、ウイルス安全性を向上させることが可能です。インプロセスパラメータでウイルスクリアランスを的確に評価できるかどうかを実証するには、広範囲の試験が必要です。そのような試験には、Q-PCRが利用可能です。ある企業のデータを、別の企業が特許申請の裏付けに使うことは不可能ですが、こうした研究の成果はバイオテクノロジー業界にとって貴重な情報となります。
参考文献
1. Smith T., Oral Presentation. PDA/FDA Viral Clearance Forum, Oct 2001.
2. Brorson, K., et al. Identification of Protein A media performance attributes that can be monitored as surrogates for retrovirus clearance during extended re-use, J. Chromagr. A 989 155?163 (2003).
3. Norling, L., Impact of multiple re-use of anion exchange chromatography media on virus removal. J. Chromagr. A 1069 79?89 (2005).
4. Curtis, S., Generic/Matrix Evaluation of X-MuLV and SV40 Clearance by Anion Exchange Chromatography in Flowthrough Mode. Oral presentation at IBC’s 8th International Conference on Process Validation for Biologicals, March 7?8, 2005, San Diego, CA.
略語
SV40=Simian Virus 40 (シミアンウイルス)
X-MuLV=Murine Leukemia Virus, Xenotropic (異種指向性マウス白血病ウイルス)
MMV=Murine Minute Virus (マウス微小ウイルス)

