Capto™ adhere
モノクローナル抗体製造のための2ステップ精製プロセス

アップストリーム技術が改良され、タンパク質の発現レベルやフィード量の増加に伴い、ダウンストリーム工程の改善が強く求められています。Capto™ adhereはマルチモーダルのBioprocess担体で、プロセススケールにおけるProtein A精製後のモノクローナル抗体(MAb)精製用に開発されました。Capto™ adhereはDNA、宿主細胞由来タンパク質(HCP)、漏出Protein A、二量体およびさらに大きな凝集体、ウイルスなどの主要な夾雑物を1ステップで除去できるため、MabSelect SuRe™と組み合せた2ステップ工程を組立てることができます。
がんや免疫学的疾患などの病気の治療用抗体のニーズは増え続けており、その需要は1年間当たり数トンレベルになっています。この要求を満たすために、今日0.1~1.0g/lであるタンパク質発現量は5g/lもしくはそれ以上に増えることが予想され、これにより培養液に含まれる不純物組成が影響を受けることが考えられます。
製造会社はまた、製造コストの削減という圧力にも直面します。モノクローナル抗体を製剤レベルまで精製するのに必要な精製ステップ数を最小限にすることは、大きな削減につながります。
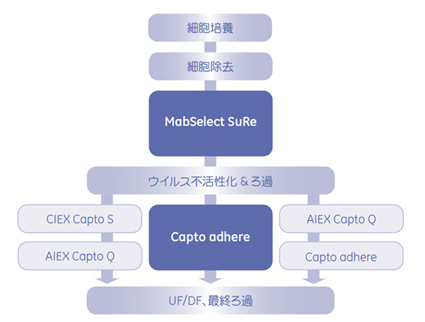
図1 Capto™ adhereを組込んだMAbの精製スキーム
凝集体を選択的に除去
Capto™ adhereはマルチモーダル強陰イオン交換体で、モノクローナル抗体の中間精製およびポリッシング用に開発されました。この新しい担体は、従来のイオン交換担体と選択性が異なります。宿主細胞由来タンパク質(HCP)の除去に加え、DNA、漏出Protein A、ウイルス、抗体の二量体および凝集体についても効果的に除去できます。抗体がカラムを素通りし、夾雑物が結合する至適条件下において、主要な夾雑物を素通りモードで除去します。添加条件の至適化には、統計学の実験計画法(DoE)の利用が最も有効です。この記事で示しているアプリケーションでは、抗体の一量体の高い回収率を維持しつつ、抗体の二量体と凝集体(D/A)レベルの減少することに着目しました。出発物質のD/A濃度は6%未満でした。回収率およびD/A除去率に対するpH(5.5~7.0)、電気伝導度(10~50 mS/cm)、添加量(100~200 mg抗体/ml担体)の影響は、DoEを用いて検討しました。予想通り、低pHでは高い回収率が得られました。一方、電気伝導度と添加量は回収率にはそれほど影響しませんでした(図2)。最も高いD/Aクリアランスは、高pHと高電気伝導度下で得られました(図3)。この結果により、高回収率(> 90%)および高D/Aクリアランス(< 1/10)が得られる添加条件を簡単に探し出すことができました。
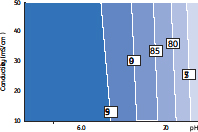
図2 回収率に対するpHの影響を示す相関図
添加濃度および電気伝導度は回収率に大きな影響を及ぼしません。pHが低いと回収率は高くなります。回収率はパーセントで表示しています(□内)。
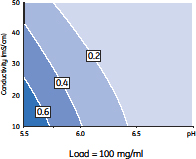
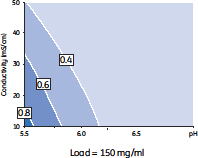
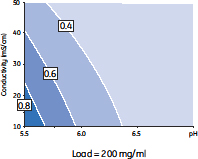
図3 凝集体クリアランスに対するpH、電気伝導度および添加濃度の影響を示す相関図
pHおよび電気伝導度を高くし、添加濃度を低くすると最も効率よく凝集体が除去できる。素通り画分中の凝集体濃度はパーセントで表示しています(□内)。
抗体の2ステップ精製
Protein A担体への結合工程では、一般に99 %という高純度が得られ、マルチモーダルの官能基を持ったCapto™ adhereとの組合せで、MabSelect SuRe™とCapto™ adhereをベースとした2ステッププロセスを組み立てることができます。モノクローナル抗体の大スケール精製プロセスは、通常3ステップ(Protein Aカラムによるアフィニティークロマトグラフィーの吸着ステップ、陽イオンと陰イオン交換体によるポリッシング)で構成されています。
イオン交換以外の選択性も有しているCapto™ adhereは、製剤レベルまで夾雑物を除去できるため、中間精製およびポリッシング両方のステップの代替となります。Capto™ adhereを2ステップ目に組み込んだ2ステップ工程で得られた回収率と純度のレベルは、3ステップ精製で得られたものと同等でした。2ステップ工程を採用することにより、一般的な3ステップ工程と比べて、プロセス時間の短縮および運転コストの削減ができます。
必要に応じて、Capto™ adhereを3ステップ工程に使用することもできます。MabSelect SuRe™、Capto™ S、Capto™ Qを用いた3ステップ工程のうちのCapto™ SをCapto™ adhereに置き換えることにより、すべての主要な夾雑物レベルを低減できます。
一般的な傾向
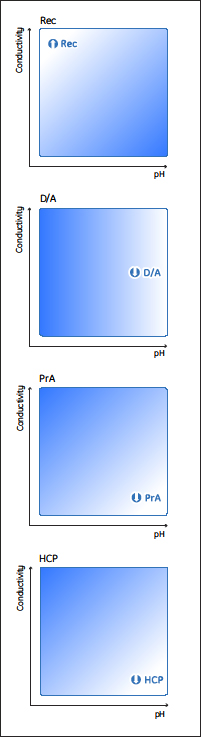
図4 添加条件(電気伝導度とpH)と回収率(Yield)ならびに凝集体(D/A)、Protein A(PrA)、HCPクリアランスの一般的な傾向
どのモノクローナル抗体も独特で、細胞株や精製工程で用いられる条件に依存して夾雑物レベルも異なります。そのため、Capto™ adhereでの精製における添加条件は、個々の抗体で最も優れた性能を発揮する条件に至適化する必要があります。検討すべき重要なパラメーターは、pH、電気伝導度、サンプル添加です。これらのパラメーターに相関関係がある可能性があるため、至適化には可能性のある相関関係をひも解くためにDoEの利用をおすすめします。
各種抗体を用いて実施したDoEにより、以下の一般的な傾向が確認されました(図4)。
・ 回収率を最大にするには、添加濃度は高く、pHは低く、電気伝導度は高くする。
・ 凝集体の除去効率を最大限にするには、pHは高く、一方で添加濃度と電気伝導度は低くする。
・ 凝集体のクリアランスは、Protein AやHCPと比較して、電気伝導度の影響を受けにくい。
・ Protein AおよびHCPのクリアランスを最大にするには、pHは高く、一方で電気伝導度と添加濃度は低くする。
これにより、最適な性能を得るには、回収率と夾雑物クリアランスのどちらかを妥協する必要があることが明らかになりました。MabSelect SuRe™とCapto™ adhereを用いた2ステップ工程で得られた5種類のMAbの至適添加条件における回収率、夾雑物のクリアランスを表1に示しています。
この表からも、至適電気伝導度は予測が困難ですが、pHは通常等電点よりも低い値をとることがわかります。
表1 異なる5種類のMAbの至適添加条件における回収率ならびに凝集体、Protein A、HCPクリアランス図
| MAb |
pI |
pH |
Conductivity (mS/cm) |
Yield (%) |
D/A (%) |
Protein A (ppm) |
HCP (ppm) |
| 1 |
~9 |
7 |
8 |
90 |
0.5 |
n.q. |
<15 |
| 2 |
8.3~8.9 |
5.5 |
3 |
95 |
0.6 |
n.q. |
2 |
| 3 |
7.5~8.4 |
6 |
2 |
95 |
0.8 |
n.q. |
9 |
| 4 |
7.7~8.0 |
7 |
20 |
91 |
0.2 |
n.q. |
0 |
| 5 |
6.5~9.0 |
7.5 |
20 |
90 |
<0.1 |
n.q. |
7.5 |
まとめ
Capto™ adhereは、モノクローナル抗体精製工程の1段階目であるProtein Aステップ後に残存する抗体の二量体や凝集体を含む夾雑物を除去することができます。この特長により、モノクローナル抗体を2ステップで精製し、プロセス時間や運転コストを削減できる可能性がでてきました。








