|
||
|---|---|---|
|
|
||
|
Location:Home > 実験手法別製品・技術情報 > 細胞周期 |
||
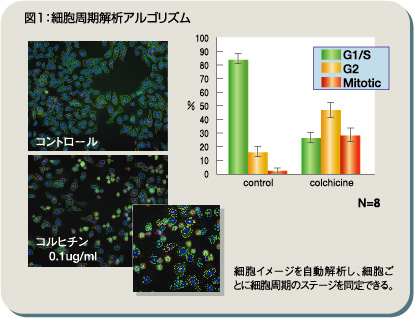
細胞イメージ解析技術がリードする遺伝子・たんぱく質の機能解析※この記事は『日経バイオビジネス 2005年3月号』に掲載された記事を日経BP社の許可を得て転載しております。そのため、社名等は当時の名称となっております。 セルファンクションイメージャー「IN Cell Analyzer」とRNA工学アマシャム バイオサイエンス株式会社が提供する「IN Cell Analyzer」は、細胞内での現象を蛍光顕微鏡イメージ画像として取得する。こうした細胞イメージ解析技術とRNAiやアプタマー技術といったRNA工学を結び付けることで、遺伝子やたんぱく質の機能解析は新たな局面を迎えることになりそうだ。その最新技術が発表された同社のフォーラムをレポートする。 目次Technology 1 siRNAを用いた細胞周期関連遺伝子の機能評価細胞周期フェーズマーカーでG2/M期を特定するまず最初に紹介されたのは、RNAiと「IN Cell Analyzer」を組み合わせた細胞周期関連遺伝子の機能評価への応用だ。細胞アッセイ試薬の進歩は、パスウェイや細胞内局在などより複雑なたんぱく質機能解析を可能にした。アマシャム バイオサイエンス株式会社では、細胞周期の中でも特にG2/M期に発現、分解されるたんぱく質としてサイクリンB1に着目。サイクリンB1のN末端部分を細胞周期フェーズマーカーとして設計し、GFPと融合してG2/M期を特定するアプローチを進めている。 「この細胞周期フェーズマーカーは、サイクリンとサイクリン依存性キナーゼ(CDK)の相互作用に関連した配列は含んでいないため、細胞周期に影響を与えません。したがって、このマーカーを使ってGFPのシグナルを追跡すれば、その細胞がいずれのステージにあるかを確認できます」と、同社テクニカルコンサルタントの畑中利彦氏は説明する。これまで生細胞解析が特に難しかったG2期、M期への解析応用も可能になってきているといえるだろう。 GFPシグナルを数値化して細胞イメージを活用同社は、G2/M期細胞周期フェーズマーカーを安定発現させたU2OS細胞株を用いて実験系を構築している。IN Cell Analyzerでは、各細胞が発するGFPシグナルを取り込み、数値化する解析アルゴリズムが確立されており、それぞれの数値に応じて各細胞がどのステージにあるかを解析できるようになっている。 実際、M期の細胞が増えるようにコルヒチン処理を施すと、GFPシグナルが細胞質から核へと移行する様子がはっきりと確認できる。「それぞれのシグナルを解析することで、各細胞のステージを自動で判別可能になっています」というように、複雑で情報量の多い細胞イメージを効率的に利用できるようIN Cell Analyzerは構築されている(図1)。
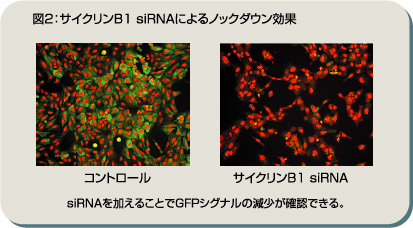
IN Cell AnalyzerによってsiRNAをスクリーニングこうした細胞イメージ解析とRNAiを組み合わせれば、細胞周期関連遺伝子の機能解析は大幅に促進される。まず同社では、Dharmacon™社のsiARRAY™の中から細胞周期に関連したsiRNA、112種類を、G2/M期細胞周期フェーズマーカーを指標にIN Cell Analyzerによってスクリーニングしている。サイクリンB1を標的としたsiRNAを導入すれば、今回のマーカーも発現が抑制され、GFPシグナルが消えることになる。それをIN Cell Analyzerで検出すれば、効率的にRNAi効果を確認できるというわけだ。 「1 nM、5 nM、50 nM、200 nMの濃度でsiRNAをU2OS細胞にトランスフェクションし、48時間後に細胞を固定。IN Cell Analyzerによってイメージを取得してRNAi効果を確認しました」というが、たとえば図2では、siRNAによるサイクリンB1のノックダウンが画像イメージから明らかに確認できる。「このようにsiRNAの導入で、GFPシグナルも消える。つまり、siRNAが機能することで細胞周期が停止されたわけですが、GFPシグナルから細胞増殖の抑制を明確に識別できることになります。さらに生体内のサイクリンB1はノックダウンされるが、細胞周期フェーズマーカーに影響を与えない配列を選択することにより、各細胞がどの周期にあるか、そのステージの分布も特定できるようになります。他の遺伝子でも同様のアプローチでRNAi効果を確認しています」。
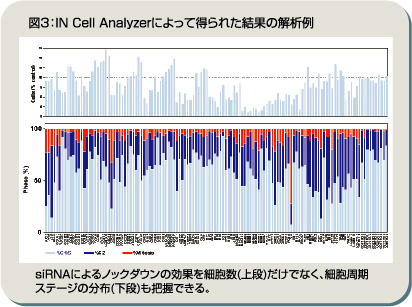
また、IN Cell Analyzerで得られたGFPシグナルを数値化し、さまざまな解析を行うことで、その現象を解析することが可能となる(図3)。細胞数やGFPのインテンシティとシグナルの局在する位置(細胞質あるいは核)をコントロールと比較し、RNAi効果を裏付けていくわけだ。
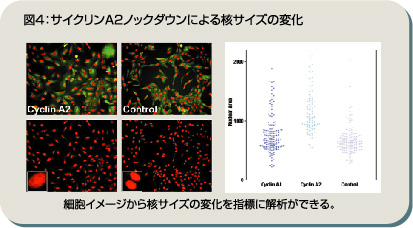
効果を確認後は、DNAマイクロアレイ「CodeLink」を用いてmRNAレベルでも解析している。DNAマイクロアレイを用いれば、サイクリンB1ノックダウンによって発現変動する関連の遺伝子も特定できる。他の遺伝子との関連性など、より詳細なサイクリンB1の機能解析へのアプローチも可能になるといえるだろう。 一つ一つの細胞に対する高度なイメージ解析「細胞数の変化を見れば、それぞれのsiRNAの効果を解析できますが、さらにG2/M期細胞周期フェーズマーカーを組み合わせることで、各細胞がどの周期にあるか、そのステージ分布まで判別できます。したがって加えたsiRNAが、細胞をどの周期でとどめるのかを確認できます」。 siRNAによって各細胞はどのような細胞周期分布を示すのか。siRNAが標的とする細胞周期関連遺伝子は、細胞内でどのように機能しているのか。畑中氏の紹介するアプローチによって、こうした知見を得られるようになるが、一つ一つの細胞に対する高度なイメージ解析技術が求められるため、なかなか進められてこなかったのが現状だ。 さらに、図4にサイクリンA2ノックダウンによる核サイズの変化を示すように、「イメージを活用したアプローチにより、核サイズの増大を視覚的に捉える」ことも可能。アマシャム バイオサイエンス株式会社の優れた試薬群と解析技術が、細胞周期解析の多彩なアプローチを実現してくれることはいうまでもないだろう。
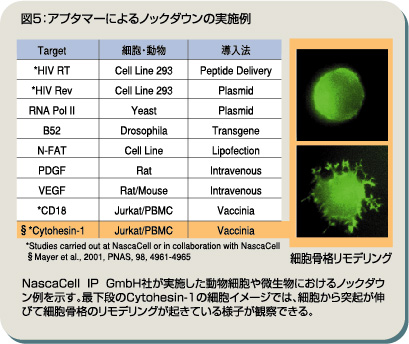
RNAiと細胞イメージ解析で標的遺伝子を見つけ出すRNAiと細胞イメージ解析を組み合わせて細胞周期解析を進めれば、創薬のターゲットとなるような遺伝子を効率的に特定することもできる。畑中氏は、その一つとしてPolo様キナーゼ(PLK)を例に挙げる。PLKは、有糸分裂を制御する遺伝子として非常によく保存されており、多くのヒトがん細胞において過剰発現している。PLKの阻害は、細胞周期をG2/M期にとどめ、がん細胞にアポトーシスを誘導することが知られている。 「siRNAによってPLKの発現を阻害すると、濃度に比例するようにM期の細胞が増加しますが、細胞のイメージからも核サイズの増大が明らかに分かります。また、アポトーシスを起こすとクロマチンが凝集するので、核シグナルのインテンシティを他の遺伝子をノックダウンした場合と比較すると、PLKの値が顕著に高くなります。PLKの阻害が、アポトーシスを有意に誘導することが確認できました」。 このようにRNAiと細胞イメージ解析による細胞周期関連遺伝子の機能評価は、多くの情報量を提供してくれる。核の大きさや細胞質のシグナル強度など、さまざまなパラメータを指標に細胞アッセイが可能で、こうしたアプローチは細胞周期関連遺伝子だけでなく、シグナル情報伝達や免疫応答関連など、あらゆる遺伝子の機能解析へと応用できる。新たな知見を生み出す技術として大きく期待されている。 Technology 2 アプタマー技術による機能解析の可能性標的たんぱく質に結合、機能阻害するアプタマーRNAi以外の応用例として、細胞イメージ解析とアプタマー技術を組み合わせた機能解析への可能性が紹介された。現在、アマシャム バイオサイエンス株式会社ではアプタマーを提供するNascaCell IP GmbH社の日本での総代理店を務めている。 アプタマーとは、標的たんぱく質に特異的に結合する20~60merのオリゴヌクレオチド(RNA/DNA)で、たんぱく質のポケット(くぼみ)に入り込んで、安定な3次元構造を形成、機能阻害する能力を有している。畑中氏は、「従来の抗体は、ターゲットたんぱくの外から結合するので、あるポイントでの機能阻害になります。その点、アプタマーは3次元構造が非常にフレキシブルになるので、たんぱく質のポケットに入り込んで、抗体とは異なる機能阻害を起こすポテンシャルを持っています」と、アプタマーへ期待を寄せる。アッセイやスクリーニングへの応用はもちろんのこと、今後、モノクローナル抗体の代替技術としての可能性も十分に秘めており、各方面で研究が進んでいる。また、結合のアフィニティに関してもnMオーダーと高い親和性を示し、「siRNAでmRNAレベルでのノックダウン、アプタマーでたんぱく質レベルでのノックダウンをするといった両方の技術を補完するような形での相乗効果が期待できる」と説明する。 アプタマーは合成、安定化、ラベル化が容易現在、アプタマーは1015のRNA/DNAライブラリーとして構築されている。アマシャム バイオサイエンス株式会社では、in vitro selection法(SELEX)によって、特異的・高親和性の配列を選択している。「たんぱく質との結合を行い、高い親和性を示すアプタマーをRT-PCRによって回収する。このサイクルを複数回行うことで、より高い特異性、親和性のアプタマーを選定していくというアプローチを採用しています」。 この時、注意しなければならないのがRNAの安定性だ。こうしたアッセイや生細胞アッセイを行う場合、分解のリスクを回避しなければならない。化学修飾によって安定性を向上させることが一般的な方法として知られているが、化学合成によって作られるアプタマーは、修飾が容易という利点を持っている。「10%FCS添加PBSの条件でも2´-OHを-NH2に置換することにより、安定性を48時間まで改善しました」というが、ごく簡単なステップで容易に安定化できるので、応用範囲は非常に広いといえるだろう。 さらに化学合成という利点を生かせば、蛍光標識やアフィニティタグの導入も簡単だ。「特定の部分に蛍光色素を導入したり、ビオチンを付加するなど、さまざまな修飾が可能です。抗体に比べて再合成も容易で、幅広いアッセイやスクリーニングへの応用が期待されます。また、毒性、抗原性がないので細胞アッセイや創薬研究という観点から見ても非常に有用な技術になります」と見据えている。 ノックダウン効果や標的タンパク質との結合をイメージで解析実際、アプタマー技術は、成長因子、ホルモン、膜たんぱく質、キナーゼなどさまざまなターゲット領域での応用研究が報告されている。具体的なアプリケーションとしては、たとえば、結合による偏光度の変化を捉える蛍光偏光法が挙げられる。蛍光標識したアプタマーを用い偏光度を測定することで、標的たんぱく質への結合能を解析したり、化合物やたんぱく質のスクリーニングに応用していくわけだ。 NascaCellIPGmbH社では、アプタマーを利用して化合物をスクリーニング、ヒット化合物の同定に成功している。また、アプタマーによるCytohesin-1を標的とした実験では、ノックダウンによって細胞骨格のリモデリングが活性化している様子がイメージから明らかに確認できる(図5)。
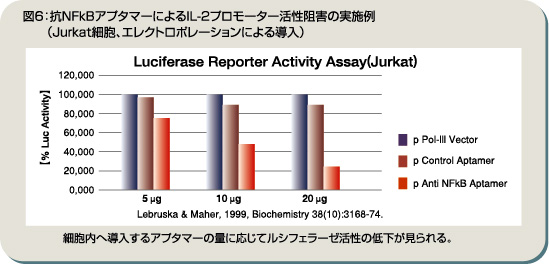
細胞内における標的たんぱく質とアプタマーの反応も、細胞イメージ解析を応用すれば視覚的に理解できる。実際に結合が起こっていれば、アプタマーと標的たんぱく質の局在イメージは重なることになる。その画像を解析すれば、細胞内でのアプタマーの結合能や阻害効果の評価に活用できる。 アプタマーの場合、抗体に比べ大きさが小さく、たんぱく質表面のくぼみにも結合できるため、たんぱく質のさまざまな部位に結合して阻害効果を示す。そのため、「基質への競合阻害だけでなく、構造変化を伴うような非競合阻害や調節ドメインの阻害など、さまざまな阻害モードに効果を示す配列を見つけ出せる可能性を秘めている」。 さまざまな導入量で阻害効果を検討する細胞への導入は、ペプチドやプラスミド、ウイルスなど一般的な方法でトランスフェクションできる。IN Cell Analyzerを利用すれば、各ベクターの導入効率を蛍光シグナルをもとに算出することも可能で、「FITCやCy5でアプタマーを標識し、プラス荷電のペプチドと混ぜることで、効率よく細胞に取り込ませることに成功しています」という。 アプタマーの導入量を変更して、阻害効果を検討することも可能だ。抗NFkBアプタマーによるIL-2プロモーター活性阻害の実施例では、アプタマーの量に比例するようにNFkBのプロモーターへの結合が阻害され、ルシフェラーゼの活性が減少することが示されている(図6)。「エレクトロポレーションによって導入していますが、ルシフェラーゼのシグナルをイメージで捉え、数値化することで、詳細な機能解析が実現します」。
細胞内の現象をイメージベースで解析していくことで、これまでは難しかった機能解析へのアプローチを実現する。フォーラムではRNAに焦点を当ててアマシャム バイオサイエンス株式会社が描くセルアナリシスが紹介されたが、今後、イメージング技術がバイオ研究に与えるインパクトの大きさは計り知れない。その最先端を同社がリードしていくことになるだろう。 お問合せフォーム※日本ポールの他事業部取扱い製品(例: 食品・飲料、半導体、化学/石油/ガス )はこちらより各事業部へお問い合わせください。 お問い合わせありがとうございます。 |
||
© 2025 Cytiva