|
||
|---|---|---|
|
|
||
|
Location:Home > 実験手法別製品・技術情報 > BIA(生物物理学的相互作用解析) |
||
BMB 2010 弊社ブース内セミナー 「生命機能をコントロールする弱い相互作用」北海道大学大学院薬学研究院 生体分子機能学研究室
T 細胞やNK 細胞に代表される免疫細胞は、その表面受容体を利用して、標的細胞表面の抗原と結合することで、最終的に免疫反応の活性、抑制を制御しています。このような細胞- 細胞、あるいは細胞- 微生物間の結合においては“弱い”相互作用がその結合を支配していることがわかってきました。この弱い相互作用の意味を読み解くための解析方法、解析例を前仲先生にお話いただきました。 免疫系における細胞- 細胞間の相互作用免疫系における細胞- 細胞間のコミュニケーションは、それぞれの細胞膜表面の間に挟まれた空間での免疫系細胞表面受容体と標的細胞表面抗原の相互作用により制御されています。これらの結合の多くは解離定数(アフィニティー)がμM 程度と弱い相互作用です。免疫系細胞表面受容体の抗原認識は、細胞膜の間の限られた空間で、さらに受容体自身やリガンドである抗原は膜にアンカーされ、通常の可溶性分子のように3次元を自由に動くことができず、膜の上を2次元的にしか動けないという制約を受けています。そのため一見弱いように見えますが、実際にはそれでも十分に結合して機能を発揮できる局所環境が作られていると考えています。また、結合に伴う速度論的パラメーターは適切なシグナル伝達を進めるために重要であると考えられます。これらの細胞間コミュニケーションは、引き続いて起こるシグナル伝達経路の開始点となっており、細胞表面で起こる現象を明らかにし、人為的に制御することで、自己免疫疾患やがん、感染症を克服する特異性の高い免疫制御が可能になると期待されています。
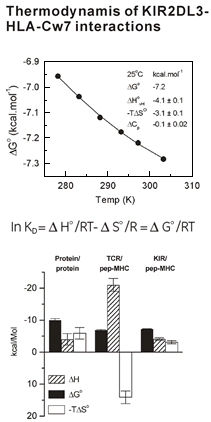
Biacore™ で温度を変化させてアフィニティーを測定すると上図のようなファントホッフの近似曲線が得られます。さらにそこからエントロピー/エンタルピーなどのパラメーターを算出することで相互作用の様式が推定できます(下図)。また本結果はITC による直接測定によりバリデートされています。 解離速度、熱力学的パラメーター測定の重要性ここでは解離定数が同じで、結合速度が異なる例をご紹介します。免疫系の細胞- 細胞間の相互作用を担う受容体としてKIR(Killer cell Immunoglobulin-like receptor)、またその比較対照としてT 細胞受容体を例に挙げます。リガンドと結合するとT細胞受容体は免疫系を活性化する方向に働き、KIRは逆に抑制の方向に働きます。これらの受容体とリガンドとの結合をBiacore™を用いて解析を行いますと、どちらも解離定数としては数μM単位になります。一方結合速度定数で見ると、代表的なT細胞受容体は2,000 M-1s-1程度、一方KIR は105 M-1s-1のオーダーなので、KIRのほうが100倍早く結合し、100倍早く離れる反応ということになります。 さらにエントロピー、エンタルピーといった熱力学的なパラメーターをBiacorを用いて算出すると、T細胞レセプターの結合はエンタルピー得、エントロピー損という結合の熱力学的特徴を示します。この特徴から、T細胞レセプターとリガンドは誘導結合していると予測されますが、実際T細胞受容体は結合にそのループ領域をリガンドMHCの形に合うように構造変化することで結合しています。一方KIRのほうはエントロピーの損がほとんどない反応です。そのメカニズムに関してはまだ明確な答えが出ていませんが結合しているがゆらゆらとしているような形でエントロピーのロスが少ないような相互作用をしているのではと考えています。 ここまでの速度論的解析と熱力学的解析をまとめて解釈するとT細胞受容体は誘導結合であり、それには構造変化を伴うためにゆっくりと結合し、さらに下流に活性化シグナルを十分に伝えるためにゆっくりと解離する。一方KIR は結合して抑制のシグナルを伝え、免疫細胞が働かないと分かったらすぐ次の細胞を標的とできるように、早く結合し、速く解離するということが考えられます。このような生命活動を担うメカニズムが、分子間の相互作用の速度、および熱力学パラメーターを測定することで見えてくるわけです。 (その他、麻疹ウイルスやLILRなどの例を挙げてご説明いただきました。)
|
||
© 2025 Cytiva