3段階精製ストラテジー【4】最終精製(Polishing)ステップ
~いよいよ千秋楽!~
原料から粗抽出したサンプル溶液には、一般的におよそ数千~1万種以上の様々なタンパク質が存在しています。前回までで、初期精製ステップにてイオン交換クロマトグラフィーに代表される“処理量とスピード”を優先した精製法により濃縮と安定化を行い、続く中間精製ステップにて異なる切り口から夾雑物を取り除き、目的タンパク質を徐々に追い詰めることをご説明してきました。
初期精製ステップを振り返りたい方はこちら
中間精製ステップを振り返りたい方はこちら
最終回の今回は、最終精製(Polishing)ステップについてご説明します。
初期精製から中間精製でほとんどの夾雑物は取り除かれていますが、フラクション中には目的タンパク質自身の構造変異体などの類似物質や核酸・ウイルス・エンドトキシンなどが微量に混入している可能性があります。最終精製の目的は、これら構造変異体や微量の夾雑物を用途に応じた許容水準まで減らすことです。
最終精製で用いられる手法は、分離能・回収率を重視して選ぶ必要があります。
多くのケースで、ゲルろ過クロマトグラフィーやイオン交換クロマトグラフィーが用いられますが、場合によっては逆相クロマトグラフィーが選択されることもあります。
それぞれの手法をこの最終精製ステップで用いる場合の注意点を見ていきましょう。
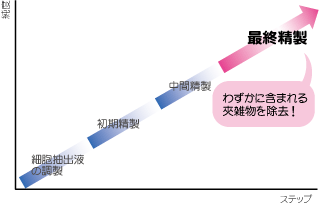
最終精製ステップで選択可能な手法
 ゲルろ過クロマトグラフィー
ゲルろ過クロマトグラフィー
分子量で分離する手法ですので、目的物が凝集して巨大分子として存在する夾雑物や、また単純に目的物の多量体などと区別して回収することが可能です。また、このワンステップで分離に加えてバッファー交換ができる利点がありますから、精製後の使用目的に合わせたバッファーを用いることで“一石二鳥”の効用を得ることが可能です。
ゲルろ過は最も操作時間がかかる分離手法の一つで、カラムサイズによってサンプルの添加量が制限されます(カラムサイズのおおよそ1/100容量が至適量)。したがって、なるべく小さいカラムを使用できるように、何らかサンプル量を減らす手法の後に行うのが理想的です。
ここで注意したいのが、遠心式の限外ろ過膜などによる機械的な“過剰濃縮”です。タンパク質によっては、ある一定の濃度を超えることにより凝集が加速する場合があります。いよいよ最終精製という段なって、せっかくの成果物が沈殿となって消えてしまっては残念ですので、濃縮は慎重に行う必要があります。
推奨担体(カラム)
可能な限り分離能の高い担体を選択することをお勧めします。
 イオン交換クロマトグラフィー
イオン交換クロマトグラフィー
非常に選択性が高いのが特徴。初期精製で利用する事も可能ですが、担体へのリガンド固定を自分で行った自作カラムや高価なカラムなどの貴重なものを用いる場合には、カラムの汚染・劣化を防ぐために中間精製で利用することをお勧めしています。吸着・溶出バッファーとも利用する担体によって様々ですが、一般に溶出後はバッファー交換が必要な場合が多いです。
初期~中間精製で多用される手法として、前回までに何度かご紹介してきました。
迅速処理・高回収量が目的の初期精製などでは、効率化のためステップワイズ溶出が汎用されるのに対し、最終精製で用いる際はできる限り高い分離・純度が重要視されるため、じっくりとグラジエント溶出を行うことを推奨します。
ゲルろ過クロマトグラフィーと同様、粒子径の小さい、高効率の担体を選択することをお勧めします。
推奨担体(カラム)
Mono Beads(粒子径10μm):ラボスケールでの高分離精製に最適です。
Source 15(粒子径15μm):最高1800cm/hでの使用が可能で、ラボスケール・ラージスケールでの高速・高分離精製に適しています。
Source 30(粒子径30μm:2000cm/hでの使用が必要なラージスケールの場合、Source15の代りに使用します。
 逆相クロマトグラフィー
逆相クロマトグラフィー
目的タンパク質が操作条件に耐えうる性質のものであれば、逆相クロマトグラフィー(RPC)の使用も可能です。RPCは疎水性の違いによりタンパク質やペプチドを分離します。通常有機溶媒を使用する方法で、非常に高い選択性と分離能を示します。タンパク質の活性や立体構造を必要としない純度チェックなどに広く用いられています。一般的に有機溶媒によってタンパク質は変性し、活性や3次元構造を取り戻すことが困難なため、RPCはタンパク質精製に適していません。しかし大半の不純物が取り除かれた最終精製において、目的タンパク質のサイズが小さく有機溶媒による変性の心配がない場合には、RPCが最良の選択と言えます。
最後に
スタート時に数千から1万もあった夾雑タンパク質は取り除かれ、最終精製を終えたフラクションにはほぼ目的タンパク質のみか、またはこの後の実験で許容できる範囲の夾雑物が残るのみとなりました。気が遠くなるような作業だな・・と思ってスタートを切った方も、戦略的に手法を組み合わせ最短コースを走る考え方を持って臨むことで、意外に短期間で終了できたかもしれません。
しかし、これからはどんどん精製の難しいタンパク質を相手に研究に取り組まれる方も多いと思います。経験者があまりいないイレギュラーなトラブルに行き当たってしまうこともあるかもしれません。試行錯誤を重ねるうちに、精製のはじめに目星を付けた“最短コース”を見失ってしまうこともあり得ます。そういうときに、この3段階精製ストラテジーを思い出し、脇道にそれず行き過ぎを防ぎながら作業を進めていただければと思います。
本連載では、初期、中期、最終精製と分けてそれぞれの過程で重要視すべき点と用いられる手法の選び方などを解説してきました。
この3つのステップを三段階精製と呼んでいますが、三段階精製では必ずしも3つの手法が必要だと言っているわけではありません。例えば、初期精製と中間精製、中間精製と最終精製を1つの手法で兼ねてしまうことができるケースや、要求される純度が低い場合は迅速な初期精製のみで精製を完了させるケースもあるからです。逆に、治療に用いられるタンパク質を精製する場合などは、最高の純度と安全性を満たすために4~5手法を組み合わせる必要があります。精製を終了するまでに用いるべき手法の数は、使用目的・純度に依存することを書き加えておきたいと思います。
弊社が作成したアプリケーション紹介シート“ApplicationNote”“Data File”などは、すべて3段階精製の考え方に則り精製ストラテジーを組み立てて、その実践結果をご紹介する形式を取っています。今後Web上などで目にされることがあれば、この3段階精製ストラテジーの意味を振り返りつつご覧いただけることと思います。
連載の総仕上げとして、その一例をご覧いただきながら終了したく思います。
ご愛読いただき、ありがとうございました。
三段階精製ストラテジー 全4回

