ヒト遺伝子治療用ウイルスの精製
ウイルスベクター
ワクチンおよびベクターの精製技術 - 目次
アデノウイルスおよびアデノ随伴ウイルスベクター
アデノウイルスは多くのヒトおよび動物特異的な血清型が存在するエンベロープのないDNAウイルスです。ヒトにおけるアデノウイルス感染は軽度の呼吸器感染を伴いますが、重篤な疾患の原因にはほとんどなりません。成人のほとんどがある程度の抗アデノウイルス抗体を有しています。
アデノウイルスは幅広く研究されており、遺伝子治療に適した以下のような優れた特長があります:1)培養による製造が容易、2)感染可能な細胞種が広い、3)アデノウイルスゲノムが染色体DNAに組み込まれるリスクが低い、4)遺伝子操作が容易で、遺伝子変異または欠損ウイルスの調製が可能、5)ウイルス粒子が壊れにくい。
アデノ随伴ウイルスはパルボウイルスの一種で小型の1本鎖DNAウイルスです。6種類のヒト血清型があり、いずれも病原性はありません。目的遺伝子の発現に持続性があるため、反復投与を減らすことができることが遺伝子治療におけるこれらベクターの主な利点です。
精製ストラテジー
アデノウイルス(AV)の分子量は一般的なタンパク質の分子量をはるかに超えます。この分子量や直径の大きさが、たとえば剪断応力に対する耐性やマストランスファーの抵抗性などの面から、供給原料の処理方法を左右します。
今日のビーズタイプのクロマトグラフィー担体の微細孔中には、このような大きな粒子は入り込むことができず、表面のみに結合します。主な戦略として、以下概要に示すように、表面積およびリガンド量を増やすために、長くて柔軟性のあるデキストラン鎖を持ったイオン交換担体を利用します。
精製プロセス
図8に清澄化細胞ライセートを出発原料とし、イオン交換によりアデノウイルスを特異的に精製するスキームの概要を紹介します。遺伝子治療やワクチンに用いるアデノウイルスや他のウイルスは、Q Sepharose™ XL virus licensed*を用いて迅速に分離でき、スケールアップも可能です。従来の遠心法と比較するとクロマトグラフィー精製は大幅な時間の短縮にもなります。例えば、最大24時間を要していたのが2、3時間にまで短縮し、回収率も高くなります。さらに、治療用のバッチサイズへのスケールアップも簡単です。図9には一般的なクロマトグラムを示します。
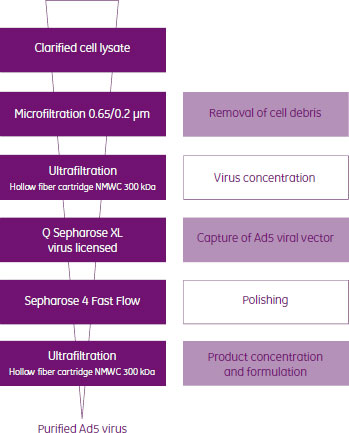
図8. アデノウイルスAd5のダウンストリームプロセス(Cobra Biomanufacturing, UKの許可を得て複製)
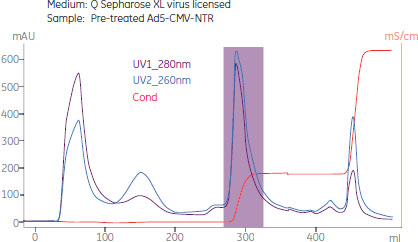
図9. Q Sepharose™ XL virus licensedイオン交換担体をベースにしたアデノウイルス精製スキーム(Cobra Biomanufacturing, UKの許可を得て複製)
アデノ随伴ウイルス(AAV2、AAV5)精製用にも、同様に堅牢で、効率的なクロマトグラフィーベースのスキームが開発されています。図11に2つのイオン交換精製工程(SP Sepharose™ High Performance、次にSOURCE™ 15Q)をベースとしたスキームの一例を紹介し、図10には第1工程のクロマトグラムを示します。
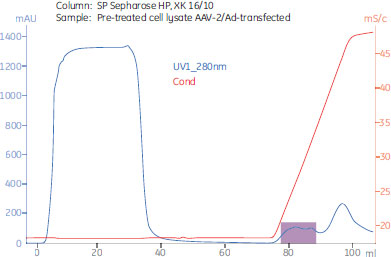
図10. SP Sepharose™ High Performanceイオン交換担体によるアデノ随伴ウイルス(AAV2)の精製(Cobra Biomanufacturing, UKの許可を得て複製)

図11. アデノ随伴ウイルス(AAV2およびAAV5)のクロマトグラフィーベースの精製スキーム
コメント
より多くのウイルスベースの遺伝子治療およびワクチン製品が臨床開発後期に移行するに従い、迅速かつスケールアップ可能なウイルスベクターの精製方法の必要性が高まっています。これは、特にアデノウイルスに当てはまります。これら2つのプロセススキームで特別に紹介した担体は、いずれも安全で、堅牢性があり、経済的な製造で要求されるニーズを満たしています。両スキームともに製造性効率の高い膜処理も取り入れています。
次へ(動物用ウイルスワクチン)



