はじめに
Biacore™ を用いて、DMSOストックされた低分子などのサンプルを測定する場合、ランニングバッファーとアナライトのDMSO濃度を一致させることが重要です。また、1%程度を超えるDMSOを用いる場合、溶媒補正(Solvent correction)を実施いただくことが多いです。
低分子化合物の測定によく選択されるPBS-P+バッファーを用いて、5% DMSO、2% DMSOを含むランニングバッファーで4点溶媒補正を行う場合の試薬調整方法を記載します。
5% DMSOを用いて4点溶媒補正を行う場合の試薬調製
Biacoreシステムによる低分子アッセイにおいて、0.05% Surfactant P20 (Tween 20) を含む10 mMまたは20 mMリン酸緩衝液の使用を推奨しています。界面活性剤を除く必要が無ければ、PBS-P+ 10 ×(0.5% P20含有)を使用し、以下の通り、ランニングバッファーや試薬を調製してください。
プロトコル
- 1.05 × PBS-P+ 2 Lの調製:10 × PBS-P+ ストック溶液210 mLをMilli-Q™ 水で2000 mLに希釈します。このバッファーは、固定化用のランニングバッファーとして、また、溶媒補正用ストック溶液、アッセイ用ランニングバッファー、サンプルの調製に使用されます。
-
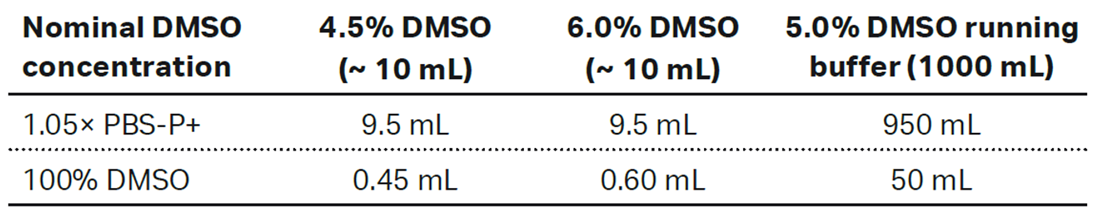
溶媒補正用ストック溶液およびアッセイ用ランニングバッファーの調製:Table 1に従い、4.5%および6.0%のDMSOを含む溶媒補正用原液を各10 mL、ならびに5%のDMSOを含むアッセイ用ランニングバッファーを1 L調製する。バッファーおよび溶液は用時調整します。
Table 1:溶媒補正用ストック溶液および5% DMSOランニングバッファー
-
4点溶媒補正溶液の調製:4.5%および6.0%のDMSOストック溶液を用いて、Table 2に従い溶媒補正溶液を調製する。溶液は用時調整します。
Table 2:4点溶媒補正溶液の調製
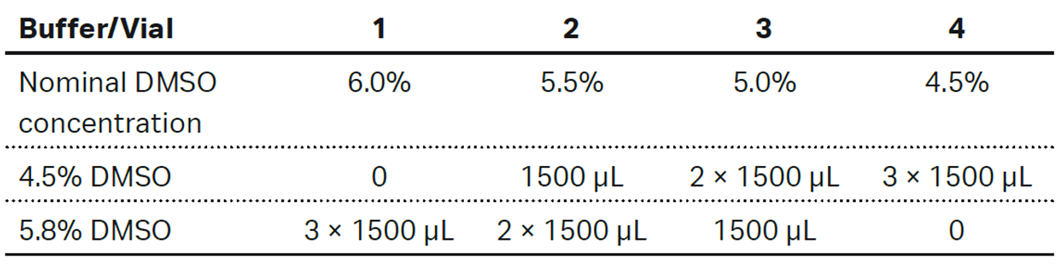 4点溶媒補正溶液は、ランニングバッファーのベースラインに対して、およそ-500 RUから+1000 RUの範囲をカバーするようにします。
4点溶媒補正溶液は、ランニングバッファーのベースラインに対して、およそ-500 RUから+1000 RUの範囲をカバーするようにします。
- アナライト調製:DMSO濃度が5%になるよう試料を調製してください。サンプルストックの濃度、凝集の傾向、およびライブラリの規模(試料数)によっては、この手順が異なる場合があります。
小~中規模の化合物ライブラリ(サンプル数が少ない場合)
例えば、サンプルストック(100% DMSO溶液)を20倍に希釈し、DMSO濃度を5%にします。1000 μLを得るには、50 μLのサンプルストックと950 μLの1.05 × PBS-P+を混合します。サンプルストックが10 mMの場合、この希釈によりサンプル濃度は500 μMとなります。
Kinetics/Affinity測定などで、濃度系列を調製するには、アッセイ用ランニングバッファー(5% DMSOを含むPBS-P+)を用いてサンプルをさらに希釈します。例をFigure 1に示します。

Figure 1:500~3.12 μMの濃度系列の希釈例
サンプルによっては、直接5% DMSOに希釈すると凝集する場合があります。そのため、追加の希釈工程が必要になることがあります。例えば、試料ストックを100% DMSOで希釈して試料濃度を下げた後、さらに1.05 × PBS-P+で希釈して5% DMSOを含む適切なサンプル濃度を調製します。
大規模の化合物ライブラリ(サンプル数が多い場合)
例えば、サンプルストック(100% DMSO溶液)を20倍に希釈し、DMSO濃度を5%にします。100 μLを得るには、5 μLのサンプルストックと95 μLの1.05 × PBS-P+を混合します。サンプルストックが10 mMの場合、この希釈によりサンプル濃度は500 μMとなります。
Kinetics/Affinity測定などで、濃度系列を調製するには、アッセイ用ランニングバッファー(5% DMSOを含むPBS-P+)を用いてサンプルをさらに希釈します。
2% DMSOを用いて4点溶媒補正を行う場合の試薬調製
Biacoreシステムによる低分子アッセイにおいて、0.05% Surfactant P20 (Tween 20) を含む10 mMまたは20 mMリン酸緩衝液の使用を推奨しています。界面活性剤を除く必要が無ければ、PBS-P+ 10 ×(0.5% P20含有)を使用し、以下の通り、ランニングバッファーや試薬を調製してください。
プロトコル
- 1.02 × PBS-P+ 2 Lの調製:10 × PBS-P+ ストック溶液204 mLをMilli-Q™水で2000 mLに希釈します。このバッファーは、固定化用のランニングバッファーとして、また、溶媒補正用ストック溶液、アッセイ用ランニングバッファー、サンプルの調製に使用されます。
-
溶媒補正用ストック溶液およびアッセイ用ランニングバッファーの調製:Table 3に従い、1.5%および3.0%のDMSOを含む溶媒補正用原液を各10 mL、ならびに2%のDMSOを含むアッセイ用ランニングバッファーを1 L調製する。バッファーおよび溶液は用時調整します。
Table 3:溶媒補正用ストック溶液および2% DMSOランニングバッファー

-
4点溶媒補正溶液の調製:1.5%および3.0%のDMSOストック溶液を用いて、Table 4に従い溶媒補正溶液を調製する。溶液は用時調整します。
Table 4:4点溶媒補正溶液の調製
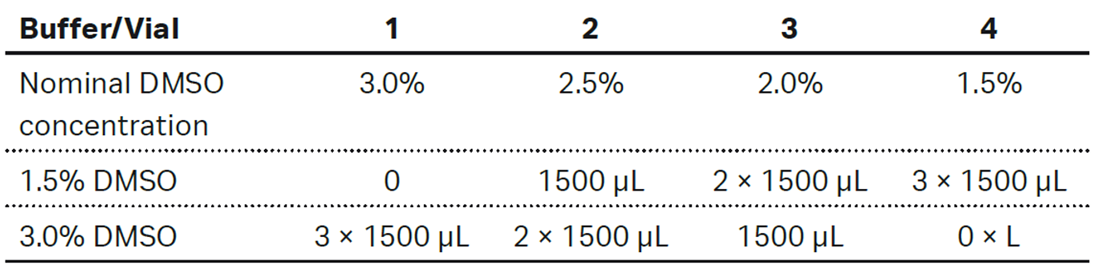 4点溶媒補正溶液は、ランニングバッファーのベースラインに対して、およそ-500 RUから+1000 RUの範囲をカバーするようにします。
4点溶媒補正溶液は、ランニングバッファーのベースラインに対して、およそ-500 RUから+1000 RUの範囲をカバーするようにします。
- アナライト調製:DMSO濃度が2%になるよう試料を調製してください。サンプルストックの濃度、凝集の傾向、およびライブラリの規模(試料数)によっては、この手順が異なる場合があります。
小~中規模の化合物ライブラリ(サンプル数が少ない場合)
例えば、サンプルストック(100% DMSO溶液)を50倍に希釈し、DMSO濃度を2%にします。1000 μLを得るには、20 μLのサンプルストックと980 μLの1.02 × PBS-P+を混合します。サンプルストックが10 mMの場合、この希釈によりサンプル濃度は200 μMとなります。
Kinetics/Affinity測定などで、濃度系列を調製するには、アッセイ用ランニングバッファー(2% DMSOを含むPBS-P+)を用いてサンプルをさらに希釈します。例をFigure 2に示します。
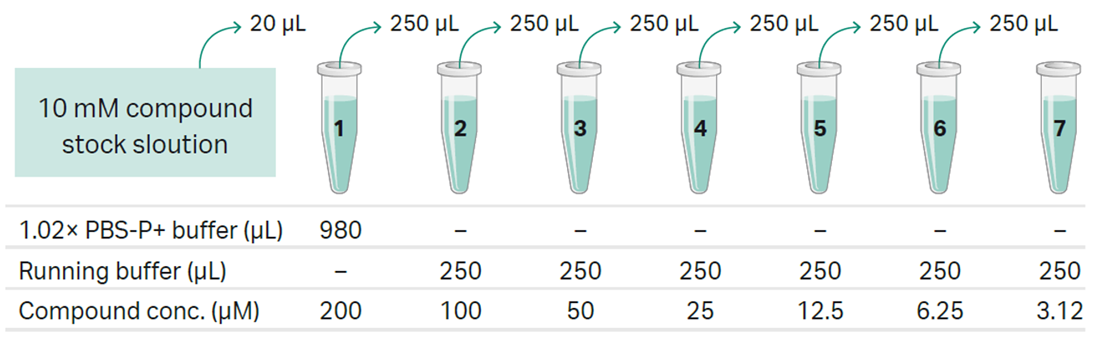
Figure 2:200~3.12 μMの濃度系列の希釈例
サンプルによっては、直接2% DMSOに希釈すると凝集する場合があります。そのため、追加の希釈工程が必要になることがあります。例えば、試料ストックを100% DMSOで希釈して試料濃度を下げた後、さらに1.02 × PBS-P+で希釈して2% DMSOを含む適切なサンプル濃度を調製します。
大規模の化合物ライブラリ(サンプル数が多い場合)
例えば、サンプルストック(100% DMSO溶液)を50倍に希釈し、DMSO濃度を2%にします。100 μLを得るには、2 μLのサンプルストックと98 μLの1.02 × PBS-P+を混合します。サンプルストックが10 mMの場合、この希釈によりサンプル濃度は200 μMとなります。
Kinetics/Affinity測定などで、濃度系列を調製するには、アッセイ用ランニングバッファー(2% DMSOを含むPBS-P+)を用いてサンプルをさらに希釈します。