|
|||||||||||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
|
|
|||||||||||||||||||
|
Location:Home > 実験手法別製品・技術情報 > タンパク質サンプル調製・前処理 |
|||||||||||||||||||
脱塩およびバッファー交換
このページの目次 手法間のメリットとデメリットの比較バッファー交換や脱塩のための手法を表1にまとめました。各手法がもつそれぞれ長所と短所、特にサンプル容量やサンプル溶液の濃度(濃縮・希釈)が手法選択のためのパラメーターとなります。
各手法についての概要透析透析チューブ膜の細孔より低分子を通過させ、バッファー交換・脱塩操作を行います。目的タンパク質の分子量と膜孔のサイズを考慮することで、不要なタンパク質の除去や分画も可能です。 【操作における一般的な注意点】
関連製品最少10 µlから透析可能 マイクロチューブタイプで、簡単で安全に透析操作を行うことができます。分画分子量・サンプル容量に合わせてご選択いただけます。 限外ろ過限外ろ過膜を用いてバッファー交換および脱塩を行うと同時に、溶液量を減らし濃縮することができます。透析膜と同様、膜孔のサイズ(数 nm~数十 nm)によって分子を分離します。 送液ポンプと組み合せて使うカセットタイプや遠心分離で操作するスピンカラムタイプがあります。(弊社ではカセットタイプのみの取扱いです) スピンカラムタイプでは20~30 ml程度、カセットタイプでは用いる送液ポンプによっても異なりますが、リットル単位での処理が可能です。 関連製品短時間で濃縮・透析が可能な限外ろ過システムです。透析や脱塩カラム処理には不向きなサンプル容量(100-2,000 ml)に対応します。 メンブレン上の滞留物・残留液量を抑えるクロスフロー型フィルターを採用しているため、1ステップで効率的に脱塩・濃縮を行えます。 ゲルろ過クロマトグラフィーゲルろ過は分離精製を行いながら適当なバッファーへの置換ができます。単に脱塩やバッファー交換が目的の場合には、ポアサイズの小さい脱塩カラムを利用したほうが簡便で、短時間で処理できます。 脱塩カラム低分子のみが通過できるポアサイズをもつゲルろ過担体(脱塩カラム)を用いて、バッファー交換および脱塩処理を行うことができます。透析法や限外ろ過法に比べて短時間で処理が可能であり、操作も非常に簡単です。 透析などに比べると急激に溶液が置換されることから、タンパク質によっては変性・沈殿形成が起こる可能性があります。不安定なタンパク質を扱う際には注意が必要です。このような場合には、2~3回に分けて徐々にバッファー組成を変化させることで、変性や沈殿形成を防げることがあります。 サンプル容量やクロマトグラフィーシステムの使用などを考慮して、適切な形状やサイズの脱塩カラムを選択します。HiTrap™ Desalting 5 mlでの脱塩処理プロトコールを下に示しますのでご参照ください。
*注意:HiTrap™ 5 ml カラムを用いる場合、5 ml/min は約120 滴/ 分(約2 滴/ 秒)に相当します。  ステップ4 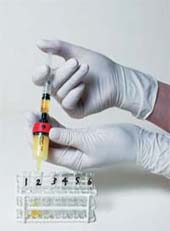 ステップ5 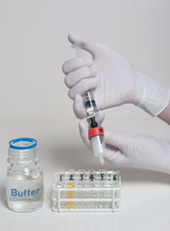 ステップ6 関連製品シリンジでも使用可能なお手軽タイプ わずか数分で脱塩処理が終了です。シリンジ・システムのどちらでも使えます。5本まで直列に接続することできます。(7.5 mlまで処理可能) サンプル容量が2.5 ~ 15 mlの脱塩に システムに連結するタイプの脱塩カラムです。同じ担体を用いているHiTrap™ Desaltingから、簡単にスケールアップができます。 自然落下型の脱塩カラムです。2.5 mlの試料容量で試料の回収率95 %以上、塩の混入率4 %以下で、希釈率はわずか1.4倍です。 沈殿/再懸濁によるバッファー交換および脱塩処理沈殿/再懸濁の手法は、脱塩と同時にサンプル溶液の濃縮や他の不純物を除きたい場合に最適です。 「処理中に沈殿しないタンパク質が存在する」、「再懸濁が難しい」などの要因からサンプルのロスが考えられるほか、沈殿法の種類によっては処理に多少の時間を要します。純粋に脱塩処理のみが目的の際には上に挙げた他の手法を用いた方がよいでしょう。 沈殿/再懸濁の詳細は 「タンパク質溶液の濃縮」に記載しました 関連製品高回収率かつ効率的に不純物を除去 TCA/アセトン沈殿をベースとした、回収率の高さが特徴のキットです。塩類の他に、界面活性剤・脂質・核酸などを効率的に除去します。 お問合せフォーム※日本ポールの他事業部取扱い製品(例: 食品・飲料、半導体、化学/石油/ガス )はこちらより各事業部へお問い合わせください。 お問い合わせありがとうございます。 |
|||||||||||||||||||
© 2026 Cytiva
 その段階でのサンプル溶液状態が、以降に行う実験またはサンプルの保存に適していない場合にはバッファー交換が必要です。中でも、サンプル溶液中から塩や荷電性の低分子物質を除去する操作を脱塩操作と呼んでいます。また、蛍光色素などでタンパク質を標識した後に、未反応の色素を除去することにも同様の手法を使うことができます。バッファー交換操作はサンプル溶液の希釈または濃縮と関連が深いため、操作後のサンプル濃度に注意する必要があります。
その段階でのサンプル溶液状態が、以降に行う実験またはサンプルの保存に適していない場合にはバッファー交換が必要です。中でも、サンプル溶液中から塩や荷電性の低分子物質を除去する操作を脱塩操作と呼んでいます。また、蛍光色素などでタンパク質を標識した後に、未反応の色素を除去することにも同様の手法を使うことができます。バッファー交換操作はサンプル溶液の希釈または濃縮と関連が深いため、操作後のサンプル濃度に注意する必要があります。