|
||
|---|---|---|
|
|
||
|
Location:Home > テクニカル情報配信サービス > バイオダイレクトメール > バイオ実験の原理と方法 |
||
イオン交換クロマトグラフィーを使いこなそう (2)分離能に関わる要因
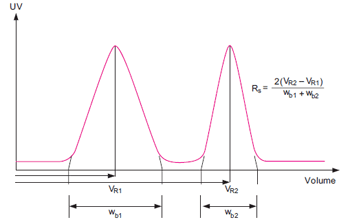
イオン交換クロマトグラフィーは、このうち電荷の違いを利用して生体分子を分離する手法です。 1960年代に確立され、微量の精製や分析からキログラム単位のプロセススケールの精製まで、サンプルを高い分離能(例えばたった1つの荷電アミノ酸の違い)で分画可能なため、タンパク質、ペプチド、核酸など電荷を持つ生体分子を精製する方法として最も普及しています。 第2回はイオン交換クロマトグラフィーの結果を左右する様々な要因について解説します。 分離能イオン交換クロマトグラフィーの分離能はカラムから溶出したピーク間の分離度(カラムの選択性) 、幅が狭く対称性の高いピークにするカラムの能力(カラム効率)を組み合わせたものです。それぞれを最適化することで高い分離が可能となります。分離能(Rs:Resolution)は2つのピークの頂点間の距離をピーク幅の平均値で割った値と定義されます。図1に示したように、Rsをクロマトグラムから求めることができます。
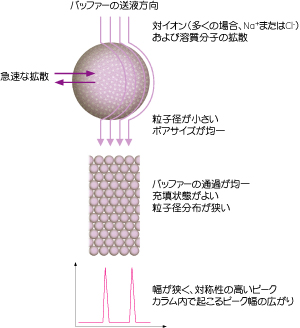
図1. 2ピーク間の分離能(Rs)の決定 カラム効率幅が狭く対称性の高いピークを溶出する能力です。幅が狭いとそれだけ分離が良いといえます。カラムの充填が不均一、充填密度が高いあるいは低い、カラム内の気泡などの原因でカラム内にバッファーの抜け道ができ、バッファーの流れが不均一になるため、ピーク幅が広がることがあります。こうした状況を回避しカラム効率を上げるポイントを図2に示します。担体の粒子径は特に重要な要素であり、適切な溶出条件でカラムの充填状態に問題がなければ、一般的に粒子径が小さいほど幅の狭いピークが得られます。ただし、粒子径の小さい担体を使用すると背圧が高くなることがあり、流速を下げる必要があるので溶出時間が長くなります。>>カラムの充填方法については「あなたにもできる!ラボスケールカラムパッキング」がおすすめです。
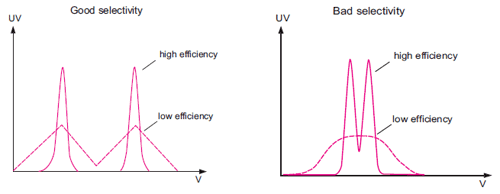
図2. カラム効率を左右する要因 カラム選択性カラム選択性は2つのピーク間の距離を示します。分離能を高くするには選択性の高い担体を選ぶことの方がカラム効率を上げるよりも重要です(図3)。イオン交換における選択性は、担体上のイオン交換基の性質や量だけでなく、バッファーのpH(タンパク質の電荷に影響する)やイオン強度、溶出条件などの実験条件にも影響を受けます。これらの実験条件の検討は容易なため、適切な担体を選びさえすれば高い分離能を得ることができます。
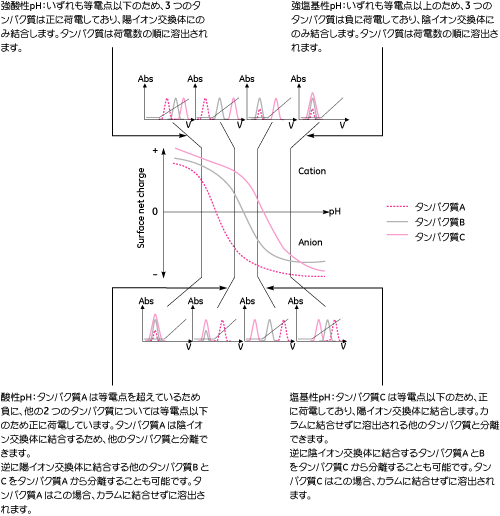
図3. 分離能に対するカラム選択性とカラム効率の影響 イオン交換クロマトグラフィーでは目的成分と夾雑物の有効電荷の差が大きいほど選択性が高くなります。図4に、pHが溶質パターンに与える影響を示します。各タンパク質の滴定曲線の間隔がもっとも大きくなるpHにおいて、反対の電荷を持つイオン交換体を使用すれば、最適の選択性が得られます。ただし滴定曲線は等電点電気泳動でゲル中の移動度からタンパク質の分子全体の有効電荷測定します。それに対しイオン交換クロマトグラフィーはタンパク質の表面の有効電荷に左右されるため、滴定曲線からタンパク質が溶出される順番を常に正しく予測できるとは限らないため、注意が必要です。
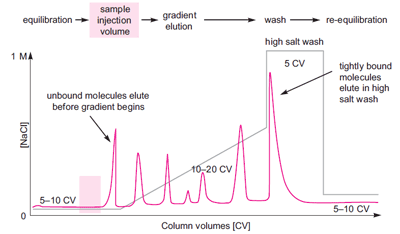
図4. タンパク質の結合・溶出パターンに対するpH の影響 溶出方法■ リニアグラジエント溶出 イオン交換クロマトグラフィーではバッファー中のイオン強度(通常は NaCl濃度)を段階的に高めていき、サンプルを溶出します。強度を高める方法にはリニアグラジエント溶出とステップワイズ溶出の2種類があります。 グラジエント溶出(図5)は、全体的なタンパク質プロフィールを確認するために、できるだけ多くの成分をカラムに結合させて順次溶出させる必要がある未知サンプルの精製や、高い分離能が要求される精製・分析に使用されます。
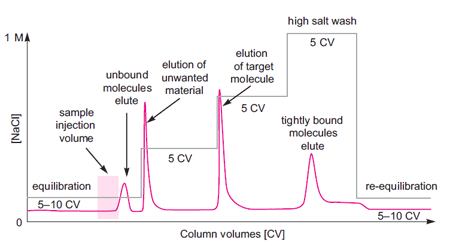
図5. グラジエント溶出による高分離分画のイオン交換クロマトグラフィーの分離例(25 ~ 45 カラム体積) ■ ステップワイズ溶出 ステップワイズ溶出にはいくつかの使い方があります。あらかじめグラジエント溶出によって溶出条件を至適化してあれば、ステップワイズ溶出に切り換えることによって、要求純度を保ったまま、分離時間を短縮し、バッファー使用量を減らすことができます(図6)。また、目的タンパク質の濃縮、夾雑物の除去の目的でも使用されます。
図6. ステップワイズ溶出によるイオン交換クロマトグラフィーの分離例(25 ~ 30 カラム体積) UV吸収とコンダクティビティーをモニタリングすることにより、タンパク質濃度と塩濃度の変化がわかります。サンプルの添加、溶出、洗浄、再平衡化に使用するバッファーの体積はカラム体積(column volume)で表します。例えば、5CVとは、担体の体積が1 ml のカラムに5 ml のバッファーを送液することを意味します。分離プロフィールのバッファー体積をカラム体積で記述しておけば、条件検討やスケールアップしたときのメソッドの移行が容易に行えます。 次回はイオン交換担体の成り立ちについて解説します。

イオン交換クロマトグラフィーを使いこなそうお問合せフォーム※日本ポールの他事業部取扱い製品(例: 食品・飲料、半導体、化学/石油/ガス )はこちらより各事業部へお問い合わせください。 お問い合わせありがとうございます。 |
||
© 2026 Cytiva
 生体分子はそれぞれ固有の特性を持っており、さまざまな性質の違いを利用することで分離・精製することができます。
生体分子はそれぞれ固有の特性を持っており、さまざまな性質の違いを利用することで分離・精製することができます。