|
|||||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
|
|
|||||||||||||
|
Location:Home > テクニカル情報配信サービス > Pharma Mail |
|||||||||||||
 IgGの精製プロセス
|
|||||||||||||
| Medium | Estimated lifetime (cycles/year)* |
|---|---|
| Sephadex™ G-25 Coarse** | 4000 |
| DEAE Sepharose™ Fast Flow** | 300 |
| Q Sepharose™ Fast Flow | 600 |
| CM Sepharose™ Fast Flow | 600 |
| CM Sepharose™ Fast Flow*** | 600 |
* Or maximum 3 years.
** Common to the albumin process.
*** For removing solvents/detergents
結果および分析
図19および20にIgGのポリアクリルアミドゲル電気泳動(PAGE)および免疫電気泳動法の結果を示します。
図21には、ゲルろ過で分析した最終製剤の純度を示しています。図22では4種類の他の市販IgGとこの方法で製造したIgGと純度を比較しています。
PAGEの結果から、IgG調製品は99%を超える純度であり、凝集体は1%未満でした。タンパク質分解酵素活性(アルギニン特異性)は1.5 U/Lで、プレカリクレイン活性(PKA)は10 IU/mL未満です。一方、欧州薬局方におけるPKA活性の限界値は35 IU/mLです。
抗捕体活性(ACA)が高かった以前の方法と比較して、この方法ではACAレベルが欧州薬局方の規定上限を大きく下回ります。3つの独立した試験場から得たACAデータおよび他のIgG分析結果を表8に示します。
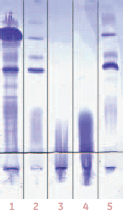
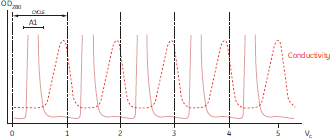
図19. IgG画分のPAGE(図16~18のクロマトグラフィーパターン参照)
1. DEAE Sepharose™ Fast Flow工程前
2. DEAE Sephcrase Fast Flow工程で得たIgG画分
3. 1回目のCM Sepharose™ Fast Flow工程で得たIgG画分
4. 最終製剤
5. Q Sepharose™ Fast Flow工程での廃液画分
PhastGel™ Gradient 8~25 gelを用いてPhastSystem™で泳動

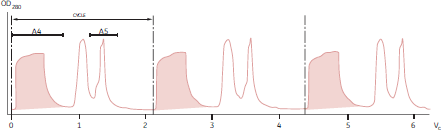
図20. この方法で製造したIgGのアガロース免疫電気泳動
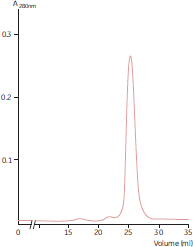
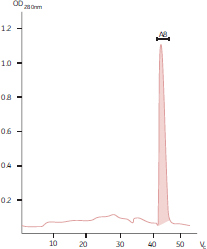
図21. Superdex™ 200ゲルろ過で分析した最終IgG画分の純度

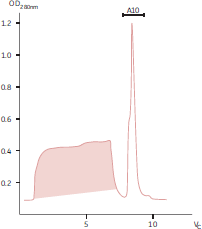
図22.PAGEによるIgG製剤純度の比較
1-4.市販IgG製剤
5. この方法で製造したIgG製剤市販IgGのうち2製品には安定化剤としてアルブミンが添加されている。
お問合せフォーム
※日本ポールの他事業部取扱い製品(例: 食品・飲料、半導体、化学/石油/ガス )はこちらより各事業部へお問い合わせください。
お問い合わせありがとうございます。
後ほど担当者よりご連絡させていただきます。
© 2026 Cytiva