
東京大学大学院
医科学研究所
津本 浩平 先生
対談:バイオ医薬品の品質管理技術の発展性~タンパク質の構造安定性の観点から~
Cytivaでコンサルティングを担当しているK.太蔵は、バイオ医薬品の開発に取り組むお客さまからの質問にお答えするために、特に品質管理に関して掘り下げる必要性を痛感していました。
そこで、バイオ医薬品の品質管理において、構造安定性をどう考えるべきか、K.太蔵は津本先生の意見を聞きに行ってみることにしました。津本先生の回答やいかに。今回は津本先生(以下、 のアイコン)とK.太蔵(以下、太蔵)の対談でお送りします。
のアイコン)とK.太蔵(以下、太蔵)の対談でお送りします。

構造安定性を決めるファクター
- 太蔵:バイオ医薬品の品質管理を考える際、その医薬品自体の構造安定性が重要なファクターとなります。もちろん活性と構造とは密接な関わりがあるので、以前の対談でも活性型の濃度をどうやって決めるのか、というお話をしていただきました。その点も含めて構造安定性を決めるファクターはどういうものか、実際に構造安定性をどのように測定評価されているのかについてお話しいただけますか。
- :構造安定性を決めるファクターというのは、どういうことですか?タンパク質側にこういう配列が必要とか、そういう意味ですか。
- 太蔵:品質管理の考え方としては、製造現場で何らかの変異が入ることによる影響や、あとは添加剤の影響です。
- :品質管理という観点においては、品質管理の検討段階に上がって来るものだとかなり構造安定性のいいものしか残っていないので、圧倒的に考えられるのは不純物の問題ですね。それが悪さをして、例えばIgG1、IgG2、IgG4の問題があって、例えばG1はFabとFcが分離しやすい、G2は鎖間シャッフリングがある、というようなことがわかっている。そのサブクラスが本質的に不安定性を決めることがあるので、それを製剤技術でどう防ぐかという検討をやっているということがありますね。安定性を決めているのは、サブクラスが同じ場合、Fab、特にCDRの配列に強く依存するので、それらがどういう振る舞いをするかを調べることが重要になるということですね。
他に、ファクターとしては製剤の条件になるpH、塩濃度、添加剤、そのタンパク製剤自身の処方濃度というのがトータルに効いてくるということになりますね。
- 太蔵:実際に評価する手法として、DSCもありますが、その他の手法も考えられますね。
- :凝集体という意味においては、ゲルろ過はもちろん、それ以外に光散乱、超遠心が実際に使われますね。ただ、これらはいずれも実際に処方されるバイアル瓶に入った状態のものをダイレクトに分析できるという系では無いので、希釈溶液にしなければいけないという問題があります。つまり、高濃度のタンパク製剤をどうやって評価するかというのは、今なお課題として残っています。実際に処方する際は、数10mgから100 mg/mlの"ドロドロ"の状態です。粘性が高い状態になっているので、それをダイレクトに評価できる系が無いのです。普通なら希釈しても物性は同じであろう、と解析するのですが、ここまで高濃度になってくると“排除体積効果”が出てしまうため、希薄溶液と同じようなデータになりません。そこも含めて考えなければならないので、皆さん困っています。現状は、これじゃなきゃいけないという方法が無いだけに、複数の方法を組み合わせて評価されていると思います。
- 太蔵:そのうちの一つがDSCであるということですね。
- :そうですね。
- 太蔵:具体的には、どんな手法との組み合わせが有効ですか?
- :組み合せを検討する場合に、こういう凝集体ができるだろうという予測が重要です。手法によって適しているサイズが異なります。例えば、モノマー、ダイマーだったらゲルろ過に勝るものは無く、もう少し大きい場合は超遠心や光散乱ですね。それより大きくなってくるとマイクロフローイメージングなど。サブミクロンくらいの大きさのパーティクルをちゃんと検出できるようなものが有効です。要するに、全部使いましょう、という話ですね。現状はどの方法がベストといえるものは必ずしも無く、皆さん模索している状態です。今後、こういう方法がいいということが確立してくると、それが一般化すると思います。
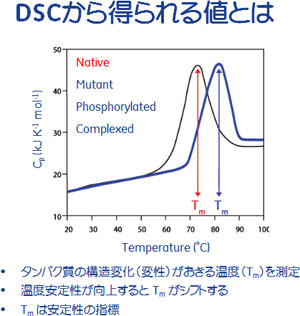
- 太蔵:DSC技術に関しては、いかがお考えですか?
- :DSCはもう既に確立していて、特に安定性そのものの評価はもちろんですが、DSCで大事なことは、だめな抗体を除けるということと思います。
それから、揺らぎがわかるというところも大事です。揺らぐということは当然ものが不安定というように見るので、物性を見るという意味では強力なツールです。
- 太蔵:揺らぎだったり、構造のエンタルピーだったり、熱容量というのは、むしろ構造学的にはすごく有用だと思いますが、現状Tmの変化だけを追いかけているところが多いのではないでしょうか?
- :Tmの変化だけであれば、CDでも見られるし、他の方法でも見られます。それに対して、DSCの強みは、崩れ出しているところとか、どういうふうに崩れるのかということがわかるという点ですね。その点に関してはプロファイルを出せということをいう場合もあるし、何故そうなるかということはともかく、あることをしたら初めのDSCのピークの立ち上がりが遅れるとか、結果的にはTmがこうなるといったデータを出しあって、おそらくこういう一般性があるのではないか等と議論し始めた状態です。この3-4年で、このピークはこうだろう、このピークはこうだろう、だからここを見たほうがいいだろうというのがわかってきている、と。
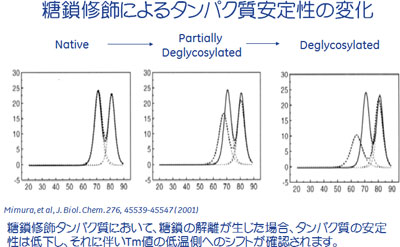
もう一つ、DSCが強いのは、凝集を与えるであろう純度に関する情報です。不純物とか、マイクロバリアントと言われるような、部分的に酸化されていたり、部分的にデリーションされていたりといった部分が見られるという点です。そういう意味でもかなり重要な技術の一つになっていると思いますね。
- 太蔵:ある意味、Tmの変化というよりは、DSCの吸熱ピークの形が重要ですね。
- :はい、ピークの形自体が大事になってきます。
- 太蔵:例えば、ある意味でDSCピークの基準の形というものが設定されて、それに対してプロファイリングする可能性はありますか。
- :可能性はあると思います。実際に論文でDSCのピークはこうなったから安定になりました、と皆さん言い出している。こういうことが認められつつあるので、もう何年か経つと明らかに品質管理のレベルで使うということになることを想定していると思っています。
- 太蔵:わかりました。
先ほど凝集はゲルろ過、超遠心、光散乱とうかがいましたが、DSCで凝集体、モノマー、ダイマー、テトラマー、そのあたりの評価を行うのはどのくらい現実的でしょうか。
- :結局、会合体、凝集体は、可逆と不可逆でも分離しますし、pH、添加剤の状況、濃度によっても分離しますので、皆さん、一生懸命データをとって、規則性を見つけ出しているところだと思います。だから、ある抗体でこういうことが言えているから、別の抗体でこうだと言えるとは限らないという厳しさがあります。まだ皆さん、このあたりは模索しているというふうに理解しています。
クラウディング状態の安定性というのは、実際は現状の抗体薬のほとんどは高濃度にしているので、高濃度で添加剤存在下での安定性、凝集性ということは考えていますが、クラウディングそのものを考えているとは限らないと思いますね。既存の性格では考えられないくらい粘性の高い、ドロドロの状態で、しかも長期保存ということをするので、そこは重要なポイントになってきます。これまでは比較的安定で処方しやすい抗体薬が多かったので、これから色々な次世代抗体や改変抗体が出てきた際に、このことはすごく重要になってくると思いますね。
- 太蔵:よくわかりました。ありがとうございます。
添加剤
- 太蔵:最後に、製剤研究につながる内容になると思いますが、界面活性剤であるとか、その他添加剤の関与のメカニズムの評価はどれくらい重要になるとお考えでしょうか。タンパク質に影響を与えるような界面活性剤やアルギニン分子のようなものがどういうメカニズムでタンパク質に相互作用して、もしくは相互作用をしていなかったら、どういう形でタンパク質と関係性を保って安定性に寄与しているのかという理解は、どこまで必要でしょうか?
- :もともと70年代から80年代の溶液論があって、それで水和に効いている、結合しているみたいなことで分けて、考えられていますね。
未だにその議論が基本になっています。ただ、各論になってきて、例えばポリエチレングリコールが凝集抑制をする際は、タンパク質にうまく結合して、疎水の領域を覆ってとこれまで言われていました。最近では、溶けているタンパク質の状態によっては、どうも水和構造が安定化する、タンパクの周りに水を集めるような効果もかなりあるということが実は言われています。
それはグリセロールも同様です。グリセロールはもともと安定化に寄与すると言われていたのが、実はポリオールが、高濃度で凝集抑制もしているということを提案している人もいます。アルギニンの話もそうですね。弱い結合をすると言われていたのが、実際、タンパク質のパッキングが良いとアミノ酸の効果で水和構造が安定化するということになっている。昔言われていた分類は基本的に正しいのですが、色々なタンパク治療薬が出てきて、どうもそれだけでは単純に理解できないとわかり、皆さん、静かに研究をしだしているという状況ですね。
- 太蔵:この分野でのITCの活用は、どのくらい現実的ですか。
- :わりと現実的ですね。
- 太蔵:活性剤とタンパク質のインタラクションですね。
- :"こういうふうに変わる"ということがわかるので、ある添加剤ではこういうエンタルピーだけれども、別の添加剤ではこういうエンタルピーになるということで、添加剤の効果が外挿できます。相互作用の時点で生じる周りの水の状況変化を反映するので、一番わかりやすいのはカロリーメーターとなりますね。
- 太蔵:希釈熱の問題もあると思うのですが、添加剤自体を滴下していって、直接、インタラクションを見ることはいかがでしょうか?
- :有力だと思います。おもしろいと思いますね。
添加剤が高濃度でどのように集合して、希釈されるとどのように薄まって、どういう溶解熱が出るかというのは、意外とわかっていません。というか、これまで測定する系が無かった。それが今のカロリーメーターでわかってきているのですが、このデータは何なの、という解釈が難しかった。
今後はこの分野での先端になってくると思いますね。集合している添加剤がどういうふうになりますか、という話題ですね。界面活性剤でミセル的な集合体が希釈される(要するに添加剤自体がグジュグジュと集まっていたものが希釈で薄まる)というようなことがわかってくると新しい展開があるかな、と思います。
- 太蔵:一部の専門家の人がそのデータを出している状況ですか?
- :既にいらっしゃると思います。これから、かなりそのことを考えなければいけないという議論になってくると思いますね。
- 太蔵:そうすると、創薬の成果に直結してきますね。
- :そうですね。モデルタンパク質で、この作用はこうじゃないかと提案されてきたのに対して、そういう作用がタンパク質の高次構造に強く依存するというのがわかってきたと。抗体でさえ、A抗体だとこうだけれども、B抗体だとこうだ、みたいになってきていて、タンパク質の置かれている構造状態そのものに強く依存するということがわかってきたのがこの10年くらいですね。
だから、80年代に言われてきたことが、色々な治療薬が出てきて、今になって改めて見直してみると、この場合はタンパク質に結合して疎水的な相互作用を抑えているかと思えば、この場合はタンパクに水を集めて水和構造が安定しているとわかってきたので、これからもっと色々なパターンがわかってくると思います。それに対して、熱の測定は非常に大きな貢献をするだろうなと思います。
- 太蔵:その製剤研究が決まった段階で、どこまでを品質管理にパラメーターとして使うかというのがその次の議論ですね。
- :はい。だからわかればわかるほど、検査とかやらなければいけないことは増えるし、実際、そうすべきだというふうに考えている人は多いですね。安全性、安全性、安全性、タンパク質の安定性、安定性、安定性、とリスクマネージが叫ばれるので、リスクマネージをすればするほど検査項目が増えていきますね。その中に溶液だとか、存在状態だとか、あるいはタンパク質そのものを分析しようという流れになっているのは確かですね。
- 太蔵:わかりました。ありがとうございました。





