|
||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
|
|
||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
|
Location:Home > 実験手法別製品・技術情報 > BIA(生物物理学的相互作用解析) > 相互作用解析の王道 |
||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
概論:タンパク質/バイオ医薬品の品質評価における、SPR/カロリメトリーの有用性目次
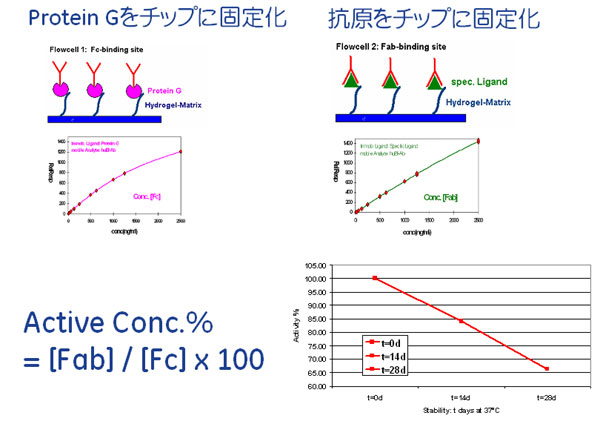
タンパク質の濃度と活性活性を持つタンパク質の濃度はどのようにして決定されるのでしょうか。タンパク質の濃度決定方法として最も一般的な方法は、Lowry法、Bradford法のような比色分析、あるいは個々のタンパク質が持つ固有のモル吸光係数を用いて吸光度から濃度を求める方法です。しかし、タンパク質溶液中に存在するすべてのタンパク質がネイティブ構造を取っているとも限りません。いずれの方法でも、活性を持つタンパク質の濃度を正確に決定するためには、活性測定等何らかの方法を用いる必要があります。それでは、ネイティブ構造を持つタンパク質のみの濃度をどの様に議論すればよいのでしょうか。これに関しては、以前、対談形式で議論させていただきましたが(参照 対談:アフィニティーを測定する際の濃度測定はどうする?)、結合活性をベースに定量できる、SPRやITCが非常に有効です。 SPRでは、センサーチップに固定化した分子に対して結合活性を示すアナライトタンパク質のみが結合レスポンスとして検出されます。よって、変性、ネイティブ構造に関わらずアナライトタンパク質すべてが結合するリガンド(たとえば、抗体に対するProtein Aなど)と、ネイティブ構造のみに対して結合するリガンド(たとえば、抗体に対する抗原など)を用意し、それぞれを用いてSPRでの定量系を構築します。すると、タンパク質全体の量と、活性型の量を別々に求めることが出来ます。このネイティブ構造の割合を算出するという考え方は、変異導入による高機能性タンパク質の設計や、バイオ医薬品の純度評価、保存状態の評価をする上で非常に重要な考え方です。(図4)
さらに、SPRでは、その技術の強みを生かした解離定数(KD)、速度定数(ka, kd)の値を用いた、活性の品質評価手法はすでに、多くのバイオ医薬品メーカーが取り入れています。翻訳後修飾の違い、部分変性、凝集などにより、SPRのセンサーグラムは大きく影響を受けます。このセンサーグラムを用いた、バイオ医薬品の性質、品質の評価は、重要な手法のひとつといえるでしょう。 一方、ITCを用いることにより、化学量論比(ストイキオメトリー、結合比ともいいます:n)と解離定数(KD)を正確に評価することが出来ます。予測された、もしくは標品に対する結合比に対する、KD値の変化は、対象タンパク質の品質の変化を明確に表すことが出来ます。KDの変化、さらには反応熱の変化は、タンパク質の持つ性質を的確に反映しているのです。これに関しては、以前の対談(対談:アフィニティーを測定する際の濃度測定はどうする?)をご覧ください。 「相互作用解析の王道」について「相互作用解析の王道」は、2009年8月よりバイオダイレクトメールでお届けしています。
バイオダイレクトメールは弊社WEB会員向けメールマガジンです。バイオダイレクトメールの配信をご希望の方は、下記リンク先からご登録をお願いいたします。 関連リンク津本先生の研究内容や論文などはこちら→津本浩平先生の研究室Webサイト お問合せフォーム※日本ポールの他事業部取扱い製品(例: 食品・飲料、半導体、化学/石油/ガス )はこちらより各事業部へお問い合わせください。 お問い合わせありがとうございます。 |
||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
© 2026 Cytiva